- 2022-10-11 08:09:00
- 1850

近日,《押注平台》发表于《Journal of Hematology & Oncology》(中科院一区,IF: 23.168)期刊,此研究由华中科技大学同济医学院附属同济医院(以下简称武汉同济医院)肿瘤科吴孔明教授团队和欧洲杯押注(以下简称押注平台生物)周鹏飞博士团队共同合作完成。
以PD-1/PD-L1抗体为代表的免疫检查点阻断药物在多种癌症的治疗中获得惊奇的效果,但总体有效率不高是关键的缺陷,而肿瘤的异质性和免疫微环境的多样性是限制疗效的主要的因素。以PD-1/PD-L1抗体为基础的联合方案有望解决单一靶点有效率低,易产生耐药性的缺点,是国际研究的前沿。押注平台生物和吴孔明教授课题组联合开发出抗鼠PD-L1和TGF-β双特异抗体(YM101),可同时阻断PD-1/PD-L1和TGFR2/TGF-β信号通路,促进效应T细胞的活化,调节肿瘤微环境,逆转免疫抑制和纤维化,在多种小鼠荷瘤模型中表现出优于PD-L1单抗的抗肿瘤效果,但对低免疫原性的免疫荒漠型(Immune-desert)小鼠肿瘤模型中疗效有限。MSA-2是全球首个口服的干扰素基因刺激因子(STING)激动剂,STING 的下游通路可以促进 APC 细胞激活和细胞因子的释放,从而促进T细胞的启动和募集,激活先天免疫系统。本研究发现YM101联合MSA-2治疗方案在免疫豁免型(Immune-excluded)和免疫荒漠型(Immune-desert)肿瘤模型中均取得了优异的治疗效果。
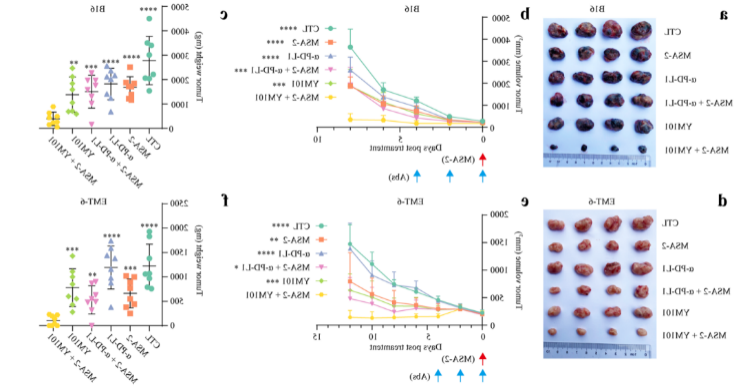
图1注:小鼠肿瘤实验示YM101联合MSA-2治疗方案拥有更强的抗肿瘤效应。
肿瘤组织的单细胞RNA测序分析结果表明YM101联合MSA-2治疗方案显著地增强小鼠体内T,NK和DC细胞等多种免疫细胞的抗肿瘤免疫反应。

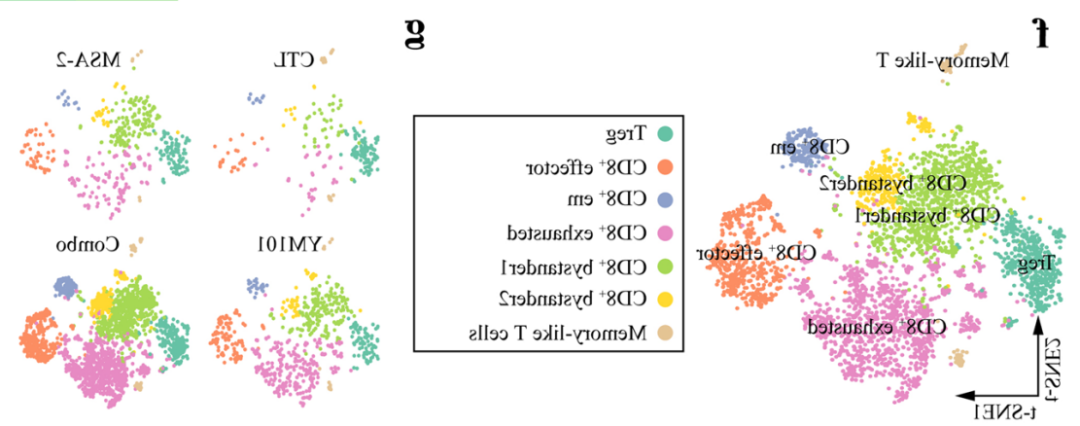
图2注:单细胞组学数据显示:联合治疗有效的重塑了肿瘤免疫微环境,增加了多种类型的T细胞亚群的丰度。
此项研究进一步证实了YM101对TGF-β高表达类型肿瘤的治疗效果,同时极大的拓宽了YM101抗肿瘤谱。基于TGF-β/ PD-L1双抗体的联合疗法也极有可能成为解决目前已有免疫治疗耐药的全新解决方案,具有很大的临床意义和转化价值。
迄今关于TGF-β/PD-L1双抗体我司已发表了3篇文章,分别从YM101单药的作用机制,以及联合治疗方向进行了研究,揭示了YM101抑制TGF-β和PD-L1的双通路协同机制,并进一步揭示了YM101联合治疗显著增强抑瘤效果,为TGF-β/PD-L1双抗体临床方案的设计提供了坚实的理论基础。
双特异性抗体是当前新药研发的风口,国内外各大制药公司均在此领域重点布局。押注平台生物通过多年的不懈努力,成功建立了具有国际自主知识产权的YBODY®和CHECKBODY™双抗体研制押注平台。目前押注平台生物已有四个药物(M802,M701,Y150,Y101D)获得中美临床批件并开展临床试验,其中基于CHECKBODY™平台构建的TGF-β/PD-L1双抗体正在开展I期临床。
相关链接:
押注平台生物PD-L1/TGF-β双特异性抗体完成临床试验首例受试者给药
J Hematol Oncol.:押注平台生物制药公司研发的基于PD-L1/TGF-β双特异抗体YM101的联合疗法抗肿瘤效果优异
J Hematol Oncol.:武汉押注平台生物制药公司研发的PD-L1/TGF-β双特异抗体YM101抗肿瘤效果优异








